Fizikte termodinamik sistemlerin incelenmesindeki önemli sorulardan biri, bu sistemin bazı yararlı işler yapıp yapamayacağı sorusudur. İş kavramıyla yakından ilgili olan iç enerji kavramıdır. Bu yazıda ideal bir gazın iç enerjisinin ne olduğunu ele alacağız ve onu hesaplamak için formüller vereceğiz.
İdeal gaz
Gaz hakkında, üzerinde dış etki altında herhangi bir elastik kuvveti olmayan ve sonuç olarak hacmini ve şeklini korumayan bir toplanma durumu olarak her okul çocuğu bilir. Birçoğu için ideal gaz kavramı anlaşılmaz ve belirsizliğini koruyor. Hadi açıklayalım.
İdeal gaz, aşağıdaki iki önemli koşulu sağlayan herhangi bir gazdır:
- Onu oluşturan parçacıkların boyutu yoktur. Bir boyutları var, ancak aralarındaki mesafelere kıyasla o kadar küçük ki, tüm matematiksel hesaplamalarda göz ardı edilebilir.
- Parçacıklar, van der Waals kuvvetleri veya kuvvetleri kullanarak birbirleriyle etkileşmezler.diğer doğa. Aslında tüm gerçek gazlarda böyle bir etkileşim mevcuttur, ancak enerjisi kinetik parçacıkların ortalama enerjisine kıyasla ihmal edilebilir.
Tarif edilen koşullar, sıcaklıkları 300 K'nin üzerinde olan ve basınçları bir atmosferi geçmeyen hemen hemen tüm gerçek gazlar tarafından karşılanır. Çok yüksek basınçlar ve düşük sıcaklıklar için gazların ideal davranıştan sapması gözlemlenir. Bu durumda, gerçek gazlardan söz edilir. Van der Waals denklemi ile tanımlanırlar.
İdeal gazın iç enerjisi kavramı
Tanıma göre, bir sistemin iç enerjisi, bu sistemin içerdiği kinetik ve potansiyel enerjilerin toplamıdır. Bu kavram bir ideal gaza uygulanırsa, potansiyel bileşen atılmalıdır. Gerçekten de, ideal bir gazın parçacıkları birbirleriyle etkileşmediğinden, mutlak boşlukta serbestçe hareket ettikleri düşünülebilir. İncelenen sistemden bir parçacığı çıkarmak için, etkileşimin iç kuvvetlerine karşı iş yapmak gerekli değildir, çünkü bu kuvvetler mevcut değildir.
Dolayısıyla, ideal bir gazın iç enerjisi her zaman kinetik enerjisiyle çakışır. İkincisi, sırayla, sistemin parçacıklarının molar kütlesi, sayıları ve ortalama öteleme ve dönme hareketi hızı ile benzersiz bir şekilde belirlenir. Hareket hızı sıcaklığa bağlıdır. Sıcaklıktaki bir artış, iç enerjide bir artışa yol açar ve bunun tersi de geçerlidir.
için formüliç enerji
İdeal bir gaz sisteminin iç enerjisini U harfi ile ifade edin. Termodinamiğe göre, sistemin entalpisi H ile basınç ve hacmin çarpımı arasındaki fark olarak tanımlanır, yani:
U=H - pV.
Yukarıdaki paragrafta, U değerinin tüm gaz parçacıklarının toplam kinetik enerjisine Ekkarşılık geldiğini öğrendik:
U=Ek.
İstatistiksel mekanikten, ideal bir gazın moleküler kinetik teorisi (MKT) çerçevesinde, bir parçacığın ortalama kinetik enerjisinin Ek1 eşit olduğu sonucu çıkar. aşağıdaki değer:
Ek1=z/2kBT.
Burada kB ve T - Boltzmann sabiti ve sıcaklığı, z - serbestlik derecesi sayısı. Ek sisteminin toplam kinetik enerjisi, Ek1 ile sistemdeki N parçacıklarının sayısı çarpılarak elde edilebilir:
Ek=NEk1=z/2NkBT.
Böylece, bir ideal gazın iç enerjisinin formülünü elde ettik, genel formda mutlak sıcaklık ve kapalı bir sistemdeki parçacık sayısı cinsinden yazılmış:
U=z/2NkBT.
Monatomik ve çok atomlu gaz
Makalenin önceki paragrafında yazılan U formülü, N taneciklerinin sayısını belirlemek zor olduğu için pratik kullanımı için elverişsizdir. Ancak, n maddesinin miktarının tanımını dikkate alırsak, bu ifade daha uygun bir biçimde yeniden yazılabilir:
n=N/NA; R=NAkB=8, 314 J/(molK);
U=z/2nR T.
z serbestlik derecesinin sayısı, gazı oluşturan parçacıkların geometrisine bağlıdır. Böylece, tek atomlu bir gaz için, z=3, çünkü bir atom bağımsız olarak uzayın yalnızca üç yönünde hareket edebilir. Gaz iki atomluysa, o zaman z=5, çünkü üç öteleme serbestlik derecesine iki dönme serbestlik derecesi daha eklenir. Son olarak, herhangi bir diğer çok atomlu gaz için, z=6 (3 öteleme ve 3 dönme serbestlik derecesi). Bunu akılda tutarak, tek atomlu, iki atomlu ve çok atomlu ideal bir gazın iç enerjisinin formüllerini aşağıdaki biçimde yazabiliriz:
U1=3/2nRT;
U2=5/2nRT;
U≧3=3nRT.
İç enerjiyi belirlemek için bir görev örneği
100 litrelik bir silindir, 3 atmosferlik bir basınçta saf hidrojen içerir. Hidrojenin belirli koşullar altında ideal bir gaz olduğunu varsayarsak, iç enerjisinin ne olduğunu belirlemek gerekir.

U için yukarıdaki formüller madde miktarını ve gazın sıcaklığını içerir. Problem durumunda, bu miktarlar hakkında kesinlikle hiçbir şey söylenmez. Sorunu çözmek için evrensel Clapeyron-Mendeleev denklemini hatırlamak gerekir. Şekilde gösterilen görünüme sahiptir.
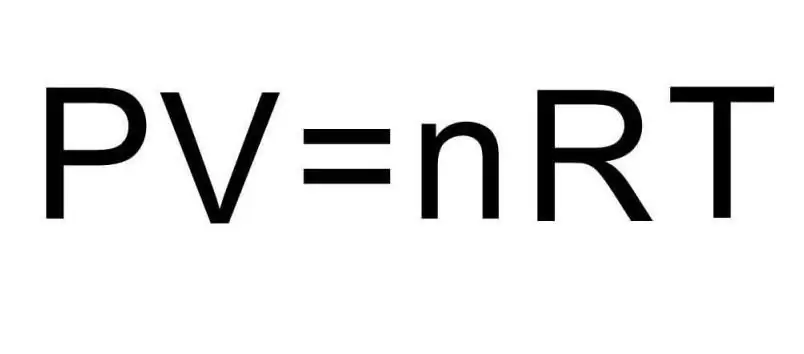
Hidrojen H2 iki atomlu bir molekül olduğundan, iç enerji formülü:
UH2=5/2nRT.
İki ifadeyi karşılaştırarak, sorunu çözmek için son formüle ulaşırız:
UH2=5/2PD.
Basınç ve hacim birimlerini koşuldan SI birim sistemine dönüştürmek, formülde karşılık gelen değerleri UH2 ile değiştirmek ve elde etmek için kalır. cevap: UH2 ≈ 76 kJ.






