Kondüktometrik analiz yöntemi, bir kimyasal reaksiyonun ilerlemesini izlemek için elektrolitik iletkenliğin ölçümüdür. Bu bilim, titrasyonun standart bir çalışma yöntemi olduğu analitik kimyada yaygın olarak uygulanmaktadır. kondüktometri nedir? Analitik kimyadaki yaygın uygulamada, bu terim titrasyon ile eşanlamlı olarak kullanılırken, aynı zamanda titrasyon dışı uygulamaları tanımlamak için de kullanılır. Bu analiz yöntemini kullanmanın faydası nedir? Genellikle bir çözeltinin genel iletkenliğini belirlemek veya iyonları içeren bir titrasyonun son noktasını analiz etmek için kullanılır.
Tarih
İletken ölçümler, Andreas Baumgartner'ın 18. yüzyılda Bad Gastein'dan gelen tuz ve maden sularınınAvusturya elektriği iletir. Böylece günümüzde su arıtma sistemlerinin etkinliğini test etmek için sıklıkla kullanılan bu yöntemin suyun saflığını belirlemek için kullanılması 1776 yılında başlamıştır. Böylece kondüktometrik analiz yönteminin tarihi başladı.
Friedrich Kohlrausch, 1860'larda suya, asitlere ve diğer çözeltilere alternatif akım uyguladığında bu bilimin gelişimini sürdürdü. Bu süre zarfında, sülfürik asit ve krom sülfat komplekslerinin etkileşimlerini inceleyen Willis Whitney, ilk kondüktometrik son noktayı buldu. Bu bulgular potansiyometrik titrasyonla ve 1883'te Robert Behrend tarafından klorür ve bromür HgNO3 titrasyonunda hacimsel analiz için ilk cihazla sonuçlandı. Bu nedenle, modern kondüktometrik analiz yöntemi Behrend'e dayanmaktadır.
Bu gelişme, asit-baz ve redoks titrasyonlarının yanı sıra tuzların çözünürlüğünü ve hidrojen iyonlarının konsantrasyonunu test etmeyi mümkün kıldı. Kondüktometrik analiz yöntemi, 1909'da başlayan cam elektrotun geliştirilmesiyle geliştirildi.
Titrasyon
Kondüktometrik titrasyon, bir reaksiyon karışımının elektrolitik iletkenliğinin bir reaktif eklenerek sürekli olarak izlendiği bir ölçümdür. Eşdeğerlik noktası, iletkenliğin aniden değiştiği noktadır. İletkenlikte gözle görülür bir artış veya azalma, en yüksek düzeyde iletken olan iki iyonun, hidrojen ve hidroksit iyonlarının konsantrasyonundaki bir değişiklikle ilişkilidir. Bu methodgeleneksel indikatörlerle kullanılamayan renkli çözeltileri veya homojen süspansiyonu (örn. odun hamuru süspansiyonu) titre etmek için kullanılabilir.
Asit-baz ve redoks titrasyonları, genellikle, bitiş noktasını belirlemek için metil portakal, asit-baz titrasyonu için fenolftalein ve iyodometrik tipte bir redoks işlemi için nişasta çözeltileri gibi ortak göstergeler kullanan gerçekleştirilir. Bununla birlikte, örneğin güçlü baz NaOH ile bir HCl çözeltisini gözlemlerken, son noktayı belirlemek için bir araç olarak elektriksel iletkenlik ölçümleri de kullanılabilir.
Proton nötralizasyonu
Titrasyon ilerledikçe, protonlar su oluşturarak NaOH oluşturmak üzere nötralize edilir. Eklenen her NaOH miktarı için eşdeğer sayıda hidrojen iyonu çıkarılır. Gerçekte, hareketli H+ katyonu daha az hareketli Na+ iyonu ile değiştirilir ve titre edilen çözeltinin iletkenliği ile ölçülen hücre iletkenliği azalır. Bu, bir sodyum klorür NaCl çözeltisinin elde edilebileceği bir eşdeğerlik noktasına ulaşılana kadar devam eder. Daha fazla baz eklenirse, daha fazla Na+ ve OH- iyonu eklendikçe bir artış olur ve nötralizasyon reaksiyonu artık kayda değer miktarda H+ çıkarmaz.

Sonuç olarak, güçlü bir asit güçlü bir baz ile titre edildiğinde, eşdeğerlik noktasında iletkenlik minimuma sahiptir. Bu minimumbir titrasyonun son noktasını belirlemek için bir gösterge boyası yerine kullanılabilir. Titrasyon eğrisi, eklenen NaOH çözeltisinin hacminin bir fonksiyonu olarak ölçülen iletkenlik veya iletkenlik değerlerinin bir grafiğidir. Titrasyon eğrisi, denklik noktasını grafik olarak belirlemek için kullanılabilir. Kondüktometrik analiz yöntemi (ve kullanımı) modern kimyada son derece önemlidir.
Reaksiyon
Zayıf asit-zayıf baz arasındaki bir reaksiyon için, elektriksel iletkenlik önce bir miktar azalır, çünkü az sayıda mevcut H+ iyonu kullanılır. Daha sonra tuz katyonu ve anyonun katkısı nedeniyle eşdeğerlik noktasının hacmine kadar iletkenlik biraz artar (güçlü bir asidik baz olması durumunda bu katkı ihmal edilebilir ve orada dikkate alınmaz.) Eşdeğerlik noktasına ulaşıldıktan sonra, OH iyonlarının fazlalığı nedeniyle iletkenlik hızla artar.
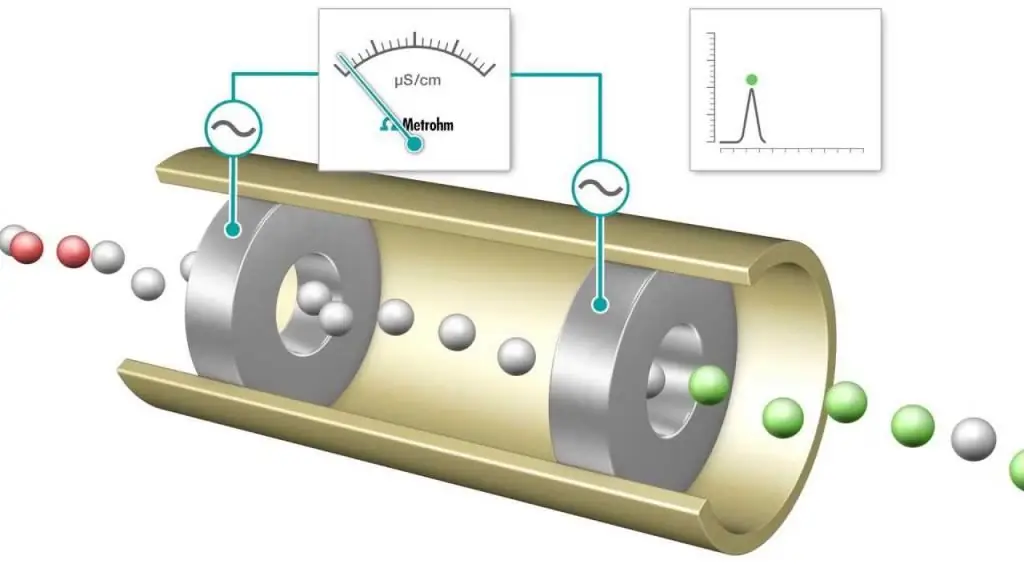
İletkenlik dedektörleri (kondüktometrik analiz yöntemi), sulu çözeltilerdeki elektrolit konsantrasyonlarını ölçmek için de kullanılır. Çözeltinin iletkenliğini oluşturan analitin molar konsantrasyonu, çözeltinin ölçülen elektrik direncinden elde edilebilir.
Kondüktometrik analiz yöntemi: prensip ve formüller
(2.4.13) C=Constcell1Λm1Res burada Constcell, ölçüm hücresine bağlı olarak sabit bir değerdir, Res, cihaz tarafından ölçülen elektrik direncidir (Ohm yasasına göre Res=I / V ve sabit bir değerle voltaj V ölçümü I yoğunluğu, Res'i hesaplamanıza izin verir) ve Λm eşdeğerdiriyonik parçacıklar için iletkenlik. Pratik amaçlar için Λm sabit olarak kabul edilebilmesine rağmen, Kohlrausch yasasına göre konsantrasyona bağlıdır:
(2.4.14)=Хт Λm0-ΘC, burada Θ bir sabittir ve Λm0 her iyonun sınırlayıcı molar iletkenlik özelliğidir. Molar iletkenlik ise sıcaklığa bağlıdır.
Yazı
Kondüktometrik ölçüm analizi yönteminin geliştirilmesi, bilim insanlarını yeni keşiflere yönlendirdi. Bilim adamları, CI iyonlarının kaynağı olarak alkil klorür hidrolizini kullanarak, Ag+ iyonlarını aşan homojen bir AgCl çökeltme sisteminde kondüktometri kullanarak kritik aşırı doygunluk oranını, Scrit'i belirlediler." Scrit=1.51, 1.73 ve 1.85'i sırasıyla 15, 25 ve 35°C'de buldular, burada tanımları gereği S=([Ag+][Cl-] / Ksp) 1/2. Aşırı doygunluk faktörünün bu tanımı bizimkine dönüştürülürse (S=[Ag+][Cl-] / Ksp), sonuçlar bu çalışmanın sonuçlarıyla oldukça iyi bir uyum içinde sırasıyla 2.28, 2.99 ve 3.42'dir. Bununla birlikte, Scrit'in sıcaklığa bağımlılığı, bu çalışmada açıklananın tam tersidir. Bu çelişkinin nedeni açık olmamakla birlikte, artan sıcaklıkla Scrit'teki azalma oldukça makul olabilir, çünkü çekirdeklenme hızı ΔGm/ kT'deki küçük bir değişiklikle ve dolayısıyla T ile orantılı olan ΔGm/ kT'deki küçük bir değişiklikle çarpıcı biçimde değişir. − 3 (lnSm) 2 formülüne göre (1.4.12) verilen sistemdeki sıcaklık değişimi ile hemen hemen sabit olduğu kabul edilir. Bu arada, S'nin tanımı [Ag +] [Cl -] / Ksp olmalıdır, çünkü aşırı doygunluk oranı[AgCl] monomer konsantrasyonu başlangıçta S=[AgCl] / [AgCl] (∞)=[Ag +] [Cl -] / Ksp. olarak verilir.
Tanaka ve Iwasaki
Kondüktometrik analiz yönteminin tarihi, iki ikonik Japon bilim adamı tarafından devam ettirildi. Tanaka ve Iwasaki, milisaniye düzeyinde hızlı bir süreci incelemek için yararlı olan çok kanallı bir spektrofotometre ile birlikte durdurulmuş akış yöntemini kullanarak AgCl ve AgBr parçacıklarının çekirdeklenme sürecini inceledi. Oldukça dar bir UV absorpsiyon bandına sahip bazı spesifik gümüş halojenür kompleksi AgXm'nin (m-1), 10-4 mol dm-3 düzeyinde bir AgC104 çözeltisi bir KX (X=) ile karıştırıldığında anında oluştuğunu bulmuşlardır. Cl veya Br) 10-2 ila 10-1 mol dm-3 mertebesinde çözelti, ardından geniş bir UV absorpsiyonuna ve spektrumda çok daha yavaş bir değişime sahip bir ara ürün oluşumu ile yaklaşık 10 ms'lik hızlı bozunması ara ürünün. Ara maddeyi, n molekülden oluşan monodispers çekirdekler (AgX) n olarak yorumladılar ve n'yi, C öncüsü AgXm'nin (m-1) çeşitli başlangıç konsantrasyonları için t=0'da görünen -dC/dt α Cn oranından belirlediler - (n=7 AgCl için -10, AgBr için n=3-4).

Ancak, AgXm (m − 1) öncülü durağan olmayan bir şekilde bozunduğundan, yarı-durağan çekirdeklenme teorisi bu süreçte uygulanmaz ve bu nedenle ortaya çıkan n değeri, nkritik çekirdeklerin değeri. Ara ürün monodispers çekirdekler n içeriyorsa,monomerik kompleks tarafından oluşturulduğunda, -dC/dt aC oranı korunmayabilir. n-merlerden daha küçük kümelerin dengede olduğunu varsaymazsak, ki − 1, ici − 1c1=ki, i − 1ci, birbiri ardına c1 → c2 → c3 →… → cn − 1 → cn., ve yalnızca son adım cn − 1 → cn geri döndürülemez; yani c1⇌c2⇌c3⇌… ⇌cn − 1 → cn.
Ayrıca, 2'den n-1'e kadar olan kümelerin konsantrasyonlarının ihmal edilebilir denge konsantrasyonlarına sahip olduğu varsayılmalıdır. Ancak, bu varsayımları haklı çıkarmak için hiçbir temel yok gibi görünüyor. Öte yandan, kübik AgCl19 için γ=101 mJ m − 2 ve kübik AgBr20 için γ=109 mJ m − 2 kullanarak hızlı işlemin sonunda kritik çekirdeklerin yarıçaplarını ve süperdoyma katsayılarını S hesaplamaya çalıştık, AgCl19 için n, 7-10 ve AgBr20 için 3-4 değerlerinin, monodispers çekirdeklerin boyutuna, n eşdeğer olduğunu varsayarsak. İncelemeleri basitçe onaylamaktan hayranlık duymaya kadar uzanan kondüktometrik analiz yöntemi, bir bilim olarak kimyaya yeni bir hayat verdi.
Sonuç olarak, bilim adamları aşağıdaki formülü keşfettiler: n=9 ile AgCl için r=0.451 nm ve S=105; n=4 ile AgBr için r=0.358 nm ve S=1230. Çünkü sistemleri, 25 °C'de yaklaşık 1.7-2.0 kritik bir AgCl aşırı doygunluğu elde eden Davis ve Jones'un sistemleriyle karşılaştırılabilir. AgNO3 ve KCl'nin eşit hacimlerde seyreltik sulu çözeltilerinde doğrudan karışımlı iletkenlik kullanıldığında, aşırı yüksek S değerleri gerçek aşırı doygunluk faktörlerini yansıtmayabilir.ara çekirdeklerle dengede.
UV emilimi
Geniş UV absorpsiyonlu bir ara maddeyi, durağan olmayan sıralı bir reaksiyon tarafından oluşturulan geniş boyut dağılımına sahip ortalamadan çok daha büyük çekirdeklere atfetmek daha mantıklı görünüyor. Ara çekirdeklerin sonraki yavaş değişimi, onların Ostwald'daki olgunlaşmasıyla ilgili gibi görünüyor.

Yukarıdaki bağlamda, Amerikalı kimyager Nielsen, n=dlogJ kullanarak, bulanıklık ölçümlerinden bulanıklık ölçümlerinden baryum sülfat parçacıklarının çekirdeklenmesi için benzer bir n yaklaşık 12 ve 103'ten büyük karşılık gelen bir S türetmiştir. / dlogC formülüne Becher-Dering benzeri bir teori. (1.3.37), ancak nyerine (n+ 1) vererek. Bu deneyde baryum iyonları ve sülfat iyonlarının çözeltileri doğrudan karıştırıldığından, hızlı geçici çekirdeklenme, karıştırmadan hemen sonra sona ermiş olmalıdır ve ölçülen, üretilen çekirdeklerin sonraki yavaş Ostwald olgunlaşması ve/veya füzyon hızı olabilir. Görünüşe göre, n'nin makul olmayan bir şekilde küçük değerinin ve aşırı yüksek aşırı doygunluğun nedeni budur. Bu nedenle, kapalı bir sistemde yarı-durağan çekirdeklenme elde etmek için tüketimlerine yanıt olarak onları serbest bırakan bazı monomerik tür rezervuarlarının her zaman gerekli olduğunu tekrar belirtmeliyiz. Becher-Döring teorisi de dahil olmak üzere tüm klasik çekirdeklenme teorileri, örtük olarak böyle bir koşulu varsayar. kondüktometrik tanımıanaliz yöntemi yukarıdaki yazının bölümlerinde verilmiştir.
Diğer bilim adamları, aralıktaki darbeli radyasyon tarafından üretilen hidratlı elektronlar tarafından halojenür iyonlarını serbest bırakmak için metilen halojenürün parçalandığı, metilen halojenür ve gümüş iyonları içeren suyun darbeli radyolizi ile gümüş halojenürün geçici çekirdeklenme sürecini araştırdılar. 4 ns'den 3 μs'ye kadar. Ürünlerin spektrumları, bir fotoçoğ altıcı ve çizgi kamerası kullanılarak kaydedildi ve monomerik gümüş halojenür öncüllerinin, bir zaman içinde mikrosaniyeler düzeyinde oluştuğu bulundu, ardından Tanaka ve Iwasaki tarafından gözlemlenene benzer bir çekirdeklenme süreci izlendi. Onların sonuçları, reaktanların doğrudan karıştırılmasıyla gümüş halojenürlerin çekirdeklenme sürecinin iki temel adımdan oluştuğunu açıkça göstermektedir; yani, μs düzeyinde bir monomerik öncünün oluşumu ve ardından 10 ms düzeyinde çekirdeklere geçiş. Ortalama çekirdek boyutunun yaklaşık 10 nm olduğuna dikkat edilmelidir.
Doygunluk
Çökeltme boyunca sürekli olarak jelatin çözeltisine AgNO3 ve KCl gibi yüksek konsantrasyonlarda reaktanların eklendiği açık sistemlerde AgCl partiküllerinin çekirdeklenmesi için süperdoygunluk katsayıları ile ilgili olarak Strong ve Wey31 1.029 (80°C) bildirdi - 1.260 (40°C) ve Leubner32, kritik aşırı doygunlukta AgCl tohum parçacıklarının büyüme hızının ölçülmesinden tahmin edildiği üzere 60°C'de 1.024 bildirdi. Bu, nicel analizin kondüktometrik yönteminin özüdür.
Öte yandan, açık AgBr parçacık sistemleri için bazıkritik aşırı doygunluk katsayısının tahmini değerleri, Scrit: Scrit∼ - Wey ve Strong33'e göre 70 °C'de 1.5, bir KBr'ye bir AgNO3 çözeltisi eklemenin farklı hızlarında renükleasyon eşiğinin bulunmasıyla belirlenen boyuta bağlı maksimum büyüme hızından çift jetler tarafından tohum parçacıklarının mevcudiyetinde çözelti; Scrit=25°C'de Jagannathan ve Wey34'e göre, iki jetli AgBr çökeltmesinin çekirdeklenme adımı sırasında elektron mikroskobuyla gözlemlenen minimum ortalama çekirdek boyutuna ilişkin verileriyle Gibbs-Thomson denkleminden belirlenen maksimum aşırı doygunluk faktörü olarak. Bu, kondüktometrik niceleme yöntemini uygularken çok etkilidir.

Bu Scrit değerlerini hesaplarken, γ=140 mJ m − 2 aldılar. Açık sistemlerde çekirdeklenme, reaktan çıkışlarının yakınında aşırı yüksek aşırı doygunluğa sahip yerel bir bölgede oluşturulan yeni oluşan çekirdeklerin hayatta kalma sürecine karşılık geldiğinden, kritik Sugimoto35'in açık sistemlerde (.3 8.3 nm) AgBr çekirdeklerinin maksimum yarıçapına ilişkin verilerini kübik AgBr için teorik γ (=109 mJ m − 2) kullanırsak, süperdoygunluk maksimum boyuttaki çekirdeklerle dengedeki çözünenin konsantrasyonuna karşılık gelir) 3, ardından kritik aşırı doygunluk faktörü Scrit, 25°C'de 1,36 olacağı gibi hesaplanır (y'nin 140 mJ/m2 olduğu varsayılırsa, o zaman Scrit=1,48).
Sonuç olarak, her durumda, kritik aşırı doygunluklargümüş halojenür partiküllerinin açık sistemleri, kapalı sistemlerde tipik olarak maksimum aşırı doygunlukların (muhtemelen kritik aşırı doygunluklara yakın) oldukça altındadır. Bunun nedeni, açık bir sistemin yerel bölgesinde üretilen çekirdeklerin ortalama yarıçapının kapalı bir sistemdeki rm'den çok daha büyük olmasıdır, bu muhtemelen yüksek konsantrasyonlu açık bir sistemin yerel bölgesindeki yüksek konsantrasyonlu birincil çekirdeklerin anlık füzyonundan kaynaklanmaktadır. yerel elektrolit konsantrasyonu.
Uygulama
Enzimatik işlemler sırasında sürekli kayıt için kondüktometrik titrasyon yönteminin kullanımı kapsamlı bir şekilde araştırılmış ve analiz edilmiştir. Hemen hemen tüm elektrokimyasal analitik yöntemler, elektrokimyasal reaksiyonlara (potansiyometri, voltametri, amperometri, kulometri) dayanır.
Kondüktometrik analiz yöntemi, elektrotlarda hiç elektrokimyasal reaksiyonun olmadığı veya ihmal edilebilecek ikincil reaksiyonların olduğu bir yöntemdir. Bu nedenle, bu yöntemde, sınır tabakadaki elektrolit çözeltisinin en önemli özelliği, oldukça geniş bir biyolojik reaksiyon aralığına göre değişen elektriksel iletkenliğidir.
Faydalar
Kondüktometrik biyosensörlerin ayrıca diğer dönüştürücü türlerine göre bazı avantajları vardır. Birincisi, düşük maliyetli ince film standart teknolojisi kullanılarak yapılabilirler. Bu, biyolojik materyali hareketsiz hale getirmek için optimize edilmiş bir yöntemin kullanılmasıyla birlikte, hem cihazların birincil maliyetinde hem detoplam analiz maliyeti. Yerleşik mikrobiyosensörler için, harici etkileri dengeleyen ve ölçüm doğruluğunu büyük ölçüde artıran diferansiyel ölçüm modunu gerçekleştirmek kolaydır.
Veriler, kondüktometrik biyosensörlerin büyük potansiyelini açıkça göstermektedir. Ancak bu, biyosensörlerde hala oldukça yeni bir trend, dolayısıyla ticari cihaz geliştirmenin umut verici bir geleceği var.
Yeni yöntemler
Bazı bilim adamları pKa'yı iletkenlikle ölçmek için genel bir yöntem tanımladılar. Bu yöntem yaklaşık 1932 yılına kadar (pH ölçüm yöntemleri kullanılmadan önce) yaygın olarak kullanılmıştır. Kondüktometrik yöntem sıcaklığa son derece duyarlıdır ve örtüşen pKa değerlerini ölçmek için kullanılamaz. Kromofor içermeyen numuneler için olası bir avantaj, 2,8 × 10-5 M'ye kadar çok seyreltik çözeltilerde kullanılabilmesidir. Son yıllarda lidokainin pKa'sını ölçmek için kondüktometri 87 kullanıldı, ancak elde edilen sonuç 0,7 idi. genel olarak kabul edilen pH değerinin altında birim başına.

Albert ve Çavuş ayrıca çözünürlük ölçümlerinden pKa'yı belirlemek için bir yöntem tanımladı. Yukarıda bahsedildiği gibi, çözünürlük pKa'ya bağlıdır, bu nedenle çözünürlük bir eğri üzerinde çoklu pH değerlerinde ölçülürse pKa belirlenebilir. Peck ve Benet, bir dizi çözünürlük ve pH ölçümü verilen monoprotik, diprotik ve amfoterik maddeler için pKa değerlerini tahmin etmek için genel bir yöntem tanımladı. Hansen ve Hafliger numunenin pKa'sını elde etti.dönen bir disk cihazında pH'ın bir fonksiyonu olarak başlangıçtaki çözünme hızlarından hidroliz yoluyla hızla ayrışır. Sonuç, pH/UV sonucuyla iyi uyum sağlar, ancak ayrışma ikinci yöntemi zorlaştırır. Bu, genel olarak kondüktometrik analiz yönteminin bir açıklamasıdır.






