Maddenin gaz halinde toplu halinin termodinamiği, sistemlerdeki termodinamik dengeyi ve yarı statik geçişleri inceleyen önemli bir fizik dalıdır. Sistemlerin davranış tahminlerinin dayandığı ana model ideal gaz modelidir. Kullanımı ile Mendeleev-Clapeyron denklemi elde edildi. Makalede düşünün.
İdeal gaz
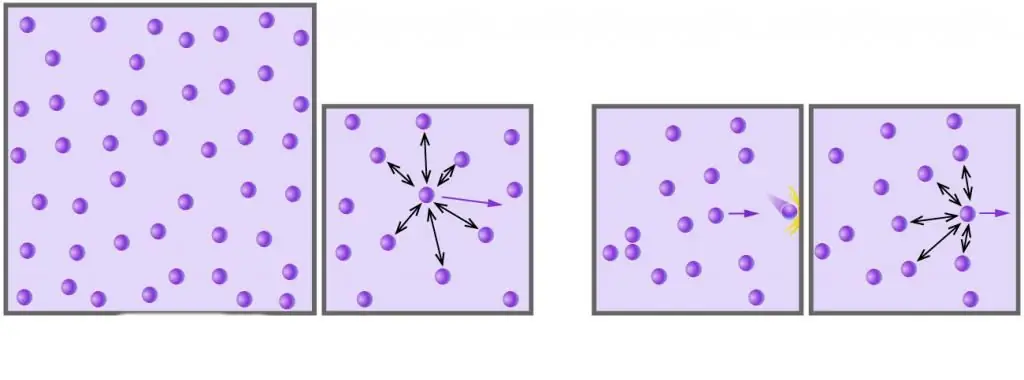
Bildiğiniz gibi, tüm gerçek gazlar, düşük basınçlarda boyutlarına kıyasla aralarındaki mesafe çok büyük olan moleküller veya atomlardan oluşur. Ek olarak, yüksek sıcaklıklarda, mutlak bir ölçekte, moleküllerin kinetik enerjisi, zayıf dipol-dipol etkileşimleriyle ilişkili potansiyel enerjilerini aşar (bu etkileşimlere ek olarak, örneğin iyonik veya hidrojen, daha sonra iç sistem enerjisinin potansiyel bileşenine önemli bir katkı sağlarlar).
NedeniyleNormale yakın koşullar altında birçok gerçek gaz için iç etkileşimleri ve parçacık boyutları ihmal edilebilir. Bu iki ana yaklaşım ideal gaz modelini oluşturur.
Mendeleev'in fizikteki denklemi

Bu denklemi Clapeyron-Mendeleev yasası olarak adlandırmak daha doğru ve adildir. Gerçek şu ki, ilk olarak 1834'te Fransız mühendis Emile Clapeyron tarafından kaydedildi. Bunu, 19. yüzyılın başlarında keşfedilen Boyle-Mariotte, Gay-Lussac ve Charles'ın gaz yasalarını analiz ederek yaptı.
Rus kimyager Dmitry Mendeleev'in değeri, denkleme modern ve kullanımı kolay bir matematiksel form vermesi gerçeğinde yatmaktadır. Özellikle Mendeleev denkleme tüm gazlar için bir sabit R=8, 314 J/(molK) eklemiştir. Clapeyron, hesaplama sürecini zorlaştıran bir dizi ampirik sabit kullandı.
Mendeleev-Clapeyron denklemi şu şekilde yazılır:
PV=nRT.
Bu eşitlik, ifadenin solundaki basınç P ve hacim V'nin çarpımının her zaman mutlak sıcaklık T ve sol taraftaki n madde miktarının çarpımı ile orantılı olduğu anlamına gelir.
Çalışılan ifade, dört parametresinden ikisini düzeltirseniz herhangi bir gaz yasasını elde etmenizi sağlar. İzoprosesler söz konusu olduğunda, çevre ile madde alışverişinin olmadığı (n=const) kapalı sistemler incelenir. Bu işlemler, tek bir sabit termodinamik parametre (T, P veya V) ile karakterize edilir.

Örnek problem
Şimdi Mendeleev-Clapeyron denklemindeki problemi çözelim. 500 gram ağırlığındaki oksijenin 2 atmosfer basınçta 100 litre hacimli bir silindirde olduğu bilinmektedir. Sistem termodinamik dengede olduğuna göre balondaki sıcaklık nedir.
Tanıma göre bir maddenin miktarının şu formülle hesaplandığını hatırlayın:
n=m/M.
m sistemin tüm parçacıklarının kütlesi olduğunda, M onların ortalama molar kütlesidir. Bu eşitlik, Mendeleev denklemini aşağıdaki biçimde yeniden yazmamızı sağlar:
PV=mRT/M.
Bu görevin çalışma formülünü nereden alıyoruz:
T=PVM/(mR).
Tüm miktarları SI birimlerine dönüştürmek ve bunları şu ifadeye dönüştürmek için kalır:
T=21013250, 10, 032/(0, 58, 314)=156 K.
Hesaplanan sıcaklık -117 oC. Bu sıcaklıkta oksijen hala gaz halinde olmasına rağmen (-182.96 oC'de yoğunlaşır), bu koşullar altında ideal gaz modeli yalnızca hesaplanan değerin kalitatif bir tahminini elde etmek için kullanılabilir.






