Fizikte gazların davranışını incelerken, izoproseslere, yani bir termodinamik parametrenin korunduğu sistemin durumları arasındaki bu tür geçişlere çok dikkat edilir. Ancak haller arasında izoproses olmayan, doğada ve teknolojide önemli rol oynayan bir gaz geçişi vardır. Bu adyabatik bir süreçtir. Bu yazıda, gaz adyabatik üssünün ne olduğuna odaklanarak bunu daha ayrıntılı olarak ele alacağız.
Adyabatik süreç
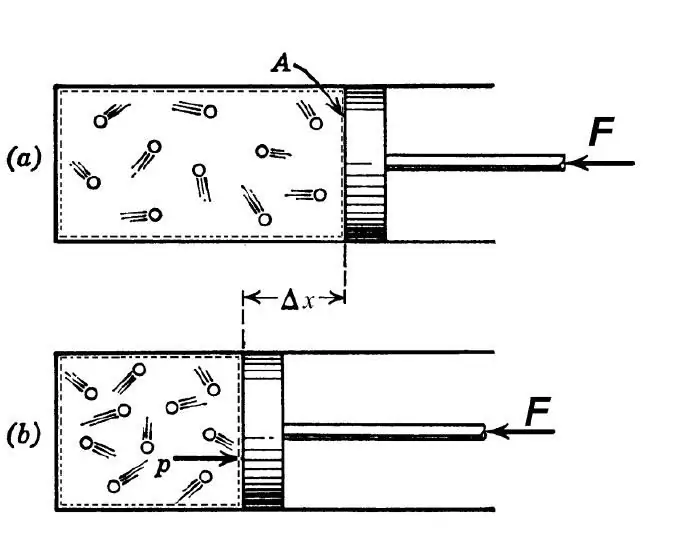
Termodinamik tanıma göre, adyabatik bir süreç, sistemin ilk ve son durumları arasında böyle bir geçiş olarak anlaşılır, bunun sonucunda dış ortam ile incelenen sistem arasında ısı alışverişi olmaz. Böyle bir işlem aşağıdaki iki koşul altında mümkündür:
- dış ortam ve ortam arasındaki ısıl iletkenliksistem şu veya bu nedenle düşük;
- işlemin hızı yüksektir, bu nedenle ısı alışverişinin gerçekleşmesi için zaman yoktur.
Mühendislikte, adyabatik geçiş hem gazı keskin sıkıştırma sırasında ısıtmak hem de hızlı genleşme sırasında soğutmak için kullanılır. Doğada, söz konusu termodinamik geçiş, bir hava kütlesinin bir yamaçtan aşağı inmesi veya yükselmesiyle kendini gösterir. Bu tür inişler ve çıkışlar havadaki çiy noktasının ve yağışın değişmesine neden olur.
Adyabatik ideal gaz için Poisson denklemi

İdeal gaz, parçacıkların yüksek hızlarda rastgele hareket ettiği, birbirleriyle etkileşmediği ve boyutsuz olduğu bir sistemdir. Böyle bir model, matematiksel açıklaması açısından çok basittir.
Adyabatik bir sürecin tanımına göre, aşağıdaki ifade termodinamiğin birinci yasasına göre yazılabilir:
dU=-PdV.
Başka bir deyişle, genişleyen veya büzülen bir gaz, iç enerjisindeki dU'daki karşılık gelen bir değişiklik nedeniyle PdV çalışır.
İdeal gaz durumunda, hal denklemini (Clapeyron-Mendeleev yasası) kullanırsak şu ifadeyi elde ederiz:
PVγ=const.
Bu eşitliğe Poisson denklemi denir. Gaz fiziğine aşina olan kişiler, y'nin değeri 1'e eşitse, Poisson denkleminin Boyle-Mariotte yasasına (izotermal) gireceğini fark edeceklerdir.işlem). Bununla birlikte, herhangi bir ideal gaz türü için γ birden büyük olduğundan, denklemlerin böyle bir dönüşümü imkansızdır. γ (gama) miktarına ideal bir gazın adyabatik indeksi denir. Fiziksel anlamına daha yakından bakalım.
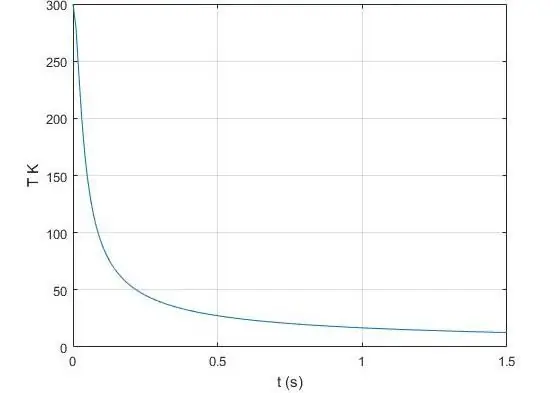
Adyabatik üs nedir?
İdeal bir gaz için Poisson denkleminde görünen γ üssü, sabit basınçta, ancak zaten sabit hacimde ısı kapasitesinin aynı değere oranıdır. Fizikte ısı kapasitesi, sıcaklığını 1 Kelvin değiştirebilmesi için belirli bir sisteme aktarılması veya sistemden alınması gereken ısı miktarıdır. İzobarik ısı kapasitesini CP sembolü ile ve izokorik ısı kapasitesini CV sembolü ile göstereceğiz. O zaman eşitlik γ:
için geçerlidir
γ=CP/CV.
Y her zaman birden büyük olduğundan, incelenen gaz sisteminin izobarik ısı kapasitesinin benzer izokorik özelliği kaç kez aştığını gösterir.
CP ve CV'nin ısı kapasiteleri
Adyabatik üssü belirlemek için, kişinin CP ve CV miktarlarının anlamını iyi bilmesi gerekir. Bunu yapmak için aşağıdaki düşünce deneyini yapacağız: Gazın katı duvarlı bir kapta kapalı bir sistem içinde olduğunu hayal edin. Kap ısıtılırsa, iletilen tüm ısı ideal olarak gazın iç enerjisine dönüştürülür. Böyle bir durumda eşitlik geçerli olacaktır:
dU=CVdT.
DeğerCVsistemi izokorik olarak 1 K ısıtmak için sisteme aktarılması gereken ısı miktarını tanımlar.
Şimdi gazın pistonu hareket eden bir kapta olduğunu varsayalım. Böyle bir sistemi ısıtma sürecinde, piston hareket ederek sabit bir basıncın korunmasını sağlar. Bu durumda sistemin entalpisi, izobarik ısı kapasitesinin ürününe ve sıcaklıktaki değişime eşit olacağından, termodinamiğin birinci yasası şu şekilde olacaktır:
CPdT=CVdT + PdV.
Buradan CP>CV olduğu görülebilir, çünkü izobarik durum değişikliği durumunda sadece sistemin sıcaklığını ve dolayısıyla iç enerjisini artırmak için değil, aynı zamanda gazın genleşmesi sırasında yaptığı işi de artırmak için ısı harcar.
İdeal bir monatomik gaz için γ değeri
En basit gaz sistemi monatomik bir ideal gazdır. Diyelim ki 1 mol gazımız var. 1 mol gazın sadece 1 Kelvin ile izobarik ısıtılması sürecinde, R'ye eşit iş yaptığını hatırlayın. Bu sembol, evrensel gaz sabitini belirtmek için yaygın olarak kullanılır. 8, 314 J / (molK)'ye eşittir. Bu durum için bir önceki paragraftaki son ifadeyi uygulayarak şu eşitliği elde ederiz:
CP=CV+ R.
İzokorik ısı kapasitesinin değerini nereden belirleyebilirsiniz CV:
γ=CP/CV;
CV=R/(γ-1).
Bir köstebek içintek atomlu gaz, izokorik ısı kapasitesinin değeri:
CV=3/2R.
Son iki eşitlikten adyabatik üssün değeri gelir:
3/2R=R/(γ-1)=>
γ=5/3 ≈ 1, 67.
Y değerinin yalnızca gazın kendi iç özelliklerine (moleküllerinin çok atomlu doğasına) bağlı olduğuna ve sistemdeki madde miktarına bağlı olmadığına dikkat edin.
Y'nin serbestlik derecesi sayısına bağımlılığı
Monatomik bir gazın izokorik ısı kapasitesi denklemi yukarıda yazılmıştır. İçinde beliren 3/2 katsayısı, bir atomdaki serbestlik derecesi sayısı ile ilgilidir. Uzayın üç yönünden sadece birinde hareket etme yeteneğine sahiptir, yani sadece öteleme serbestlik dereceleri vardır.
Sistem iki atomlu moleküllerden oluşuyorsa, üç öteleme derecesine iki dönme derecesi daha eklenir. Bu nedenle, CV ifadesi şu şekilde olur:
CV=5/2R.
O zaman γ değeri şu şekilde olacaktır:
γ=7/5=1, 4.
Diatomik molekülün aslında bir tane daha titreşim serbestlik derecesine sahip olduğuna dikkat edin, ancak birkaç yüz Kelvin'lik sıcaklıklarda aktive olmaz ve ısı kapasitesine katkıda bulunmaz.
Gaz molekülleri ikiden fazla atomdan oluşuyorsa, 6 serbestlik derecesine sahip olacaklardır. Bu durumda adyabatik üs şuna eşit olacaktır:
γ=4/3 ≈ 1, 33.
YaniBöylece bir gaz molekülündeki atom sayısı arttıkça γ değeri azalır. P-V eksenlerinde adyabatik bir grafik oluşturursanız, tek atomlu bir gazın eğrisinin çok atomlu bir gazdan daha keskin davranacağını fark edeceksiniz.
Bir gaz karışımı için adyabatik üs
Yukarıda γ değerinin gaz sisteminin kimyasal bileşimine bağlı olmadığını gösterdik. Bununla birlikte, moleküllerini oluşturan atomların sayısına bağlıdır. Sistemin N bileşenden oluştuğunu varsayalım. Karışımdaki i bileşeninin atomik kesri ai'dir. Ardından, karışımın adyabatik üssünü belirlemek için şu ifadeyi kullanabilirsiniz:
γ=∑i=1N(aiγ i).
Nerede γi i-inci bileşen için γ değeridir.
Örneğin, bu ifade havanın γ değerini belirlemek için kullanılabilir. Oksijen ve nitrojenin %99 diyatomik moleküllerinden oluştuğu için adyabatik indeksi 1.4 değerine çok yakın olmalıdır ki bu değerin deneysel olarak belirlenmesi ile doğrulanır.






