Termodinamikte, bir sistemin ilk durumundan son durumuna geçişleri incelerken, sürecin termal etkisini bilmek önemlidir. Isı kapasitesi kavramı bu etki ile yakından ilişkilidir. Bu yazıda, bir gazın izokorik ısı kapasitesi ile ne kastedildiği sorusunu ele alacağız.
İdeal gaz
İdeal gaz, parçacıkları maddesel noktalar olarak kabul edilen, yani boyutları olmayan, kütleleri olan ve tüm iç enerjisinin yalnızca moleküllerin hareketinin kinetik enerjisinden oluştuğu bir gazdır. ve atomlar.
Herhangi bir gerçek gaz ideal olarak asla açıklanan modeli karşılamayacaktır, çünkü parçacıkları hala bazı doğrusal boyutlara sahiptir ve zayıf van der Waals bağları veya başka bir tür kimyasal bağlar kullanarak birbirleriyle etkileşime girer. Bununla birlikte, düşük basınçlarda ve yüksek sıcaklıklarda, moleküller arasındaki mesafeler büyüktür ve kinetik enerjileri, potansiyel enerjiyi onlarca kez aşar. Tüm bunlar, gerçek gazlar için ideal modeli yüksek derecede doğrulukla uygulamayı mümkün kılar.
Gazın iç enerjisi
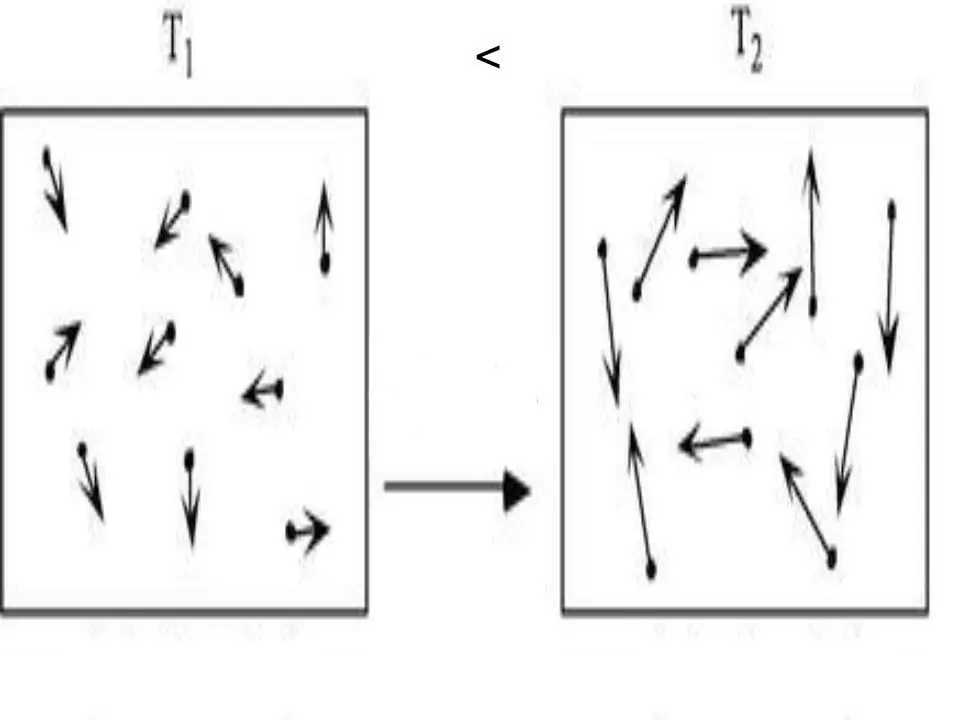
Herhangi bir sistemin iç enerjisi, potansiyel ve kinetik enerjinin toplamına eşit olan fiziksel bir özelliktir. İdeal gazlarda potansiyel enerji ihmal edilebileceğinden, onlar için eşitliği yazabiliriz:
U=Ek.
Nerede Ek kinetik sistemin enerjisidir. Moleküler kinetik teoriyi kullanarak ve evrensel Clapeyron-Mendeleev durum denklemini uygulayarak U için bir ifade elde etmek zor değildir. Aşağıda yazılmıştır:
U=z/2nRT.
Burada T, R ve n sırasıyla mutlak sıcaklık, gaz sabiti ve madde miktarıdır. Z değeri, bir gaz molekülünün sahip olduğu serbestlik derecesi sayısını gösteren bir tamsayıdır.
İzobarik ve izokorik ısı kapasitesi
Fizikte ısı kapasitesi, incelenen sistemi bir kelvin ısıtmak için verilmesi gereken ısı miktarıdır. Ters tanım da doğrudur, yani ısı kapasitesi, sistemin bir kelvin kadar soğutulduğunda saldığı ısı miktarıdır.
Bir sistem için en kolay yol, izokorik ısı kapasitesini belirlemektir. Sabit hacimdeki ısı kapasitesi olarak anlaşılır. Sistem bu şartlar altında iş yapmadığından, tüm enerji iç enerji rezervlerini arttırmaya harcanır. İzokorik ısı kapasitesini CV sembolü ile gösterelim, sonra şunu yazabiliriz:
dU=CVdT.
Yani, iç enerjideki değişimsistem sıcaklığındaki değişimle doğru orantılıdır. Bu ifadeyi bir önceki paragrafta yazılan eşitlikle karşılaştırırsak, ideal bir gazda CV formülüne ulaşırız:
СV=z/2nR.
Bu değer, sistemdeki madde miktarına bağlı olduğundan pratikte kullanılması sakıncalıdır. Bu nedenle, spesifik izokorik ısı kapasitesi kavramı, yani 1 mol gaz veya 1 kg başına hesaplanan bir değer getirildi. İlk değeri CV sembolü ile, ikinci değeri - CV sembolü ile gösterelim. m. Onlar için şu formülleri yazabilirsiniz:
CV=z/2R;
CVm=z/2R/M.
Burada M molar kütledir.
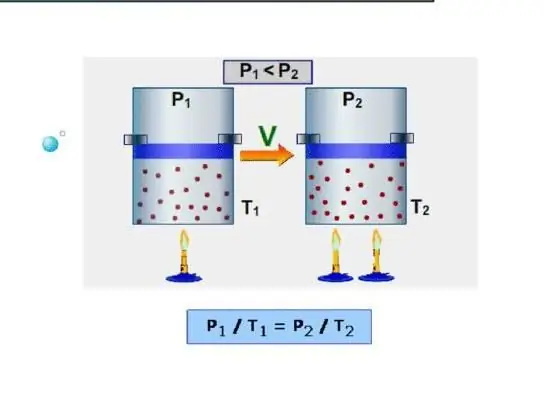
İzobarik, sistemde sabit bir basıncı korurken ısı kapasitesidir. Böyle bir işleme bir örnek, ısıtıldığında bir pistonun altındaki bir silindirdeki gazın genleşmesidir. İzokorik süreçten farklı olarak, izobarik süreçte sisteme verilen ısı, iç enerjiyi artırmak ve mekanik iş yapmak için harcanır, yani:
H=dU + PdV.
İzobarik bir sürecin entalpisi, izobarik ısı kapasitesinin ve sistemdeki sıcaklıktaki değişimin ürünüdür, yani:
H=CPdT.
Genişlemeyi 1 mol gaz sabit basıncında düşünürsek, termodinamiğin birinci yasası şu şekilde yazılır:
CPdT=CV dT + RdT.
Son terim denklemden elde edilirClapeyron-Mendeleyev. Bu eşitlikten izobarik ve izokorik ısı kapasiteleri arasındaki ilişki çıkar:
CP=CV + R.
İdeal bir gaz için, sabit basınçta özgül molar ısı kapasitesi her zaman karşılık gelen izokorik karakteristikten R=8, 314 J/(molK) kadar büyüktür.
Moleküllerin serbestlik derecesi ve ısı kapasitesi
Belirli molar izokorik ısı kapasitesinin formülünü tekrar yazalım:
CV=z/2R.
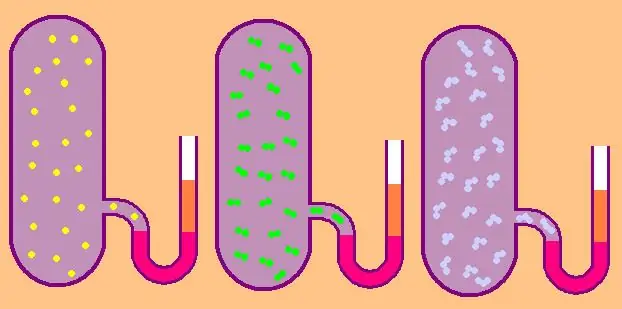
Tek atomlu bir gaz durumunda, z=3 değeri, çünkü uzaydaki atomlar yalnızca üç bağımsız yönde hareket edebilir.
Diatomik moleküllerden oluşan bir gazdan bahsediyorsak, örneğin oksijen O2 veya hidrojen H2, o zaman, öteleme hareketine ek olarak, bu moleküller hala birbirine dik iki eksen etrafında dönebilir, yani z 5'e eşit olacaktır.
Daha karmaşık moleküller için, CV
belirlemek için z=6. kullanın






