Termodinamik, fiziğin önemli bir dalıdır. Başarılarının teknolojik çağın ortaya çıkmasına neden olduğunu ve son 300 yılda insanlık tarihinin gidişatını büyük ölçüde belirlediğini güvenle söyleyebiliriz. Makale termodinamiğin birinci, ikinci ve üçüncü yasalarını ve bunların pratikteki uygulamalarını tartışıyor.
Termodinamik nedir?
Termodinamik yasalarını formüle etmeden önce, fiziğin bu bölümünün ne yaptığını bulalım.
"Termodinamik" kelimesi Yunanca kökenlidir ve "ısıdan kaynaklanan hareket" anlamına gelir. Yani, fiziğin bu dalı, termal enerjinin mekanik harekete dönüştürüldüğü ve bunun tam tersi olan herhangi bir işlemin incelenmesiyle ilgilenir.
Termodinamiğin temel yasaları 19. yüzyılın ortalarında formüle edildi. "Hareket ve ısı" bilimi, tüm sistemin davranışını bir bütün olarak ele alır, makroskopik parametrelerindeki - sıcaklık, basınç ve hacimdeki değişikliği inceler ve mikroskobik yapısına dikkat etmez. Ayrıca, birincisi yasaların formüle edilmesinde temel bir rol oynar.fizikte termodinamik. Bunların yalnızca deneysel gözlemlerden elde edildiğini belirtmek ilginçtir.
Termodinamik sistem kavramı

Bir bütün olarak kabul edilen herhangi bir atom, molekül veya diğer element grubu anlamına gelir. Her üç yasa da sözde termodinamik sistem için formüle edilmiştir. Örnekler: Dünya'nın atmosferi, herhangi bir canlı organizma, içten yanmalı bir motordaki gaz karışımı, vb.
Termodinamikteki tüm sistemler üç türden birine aittir:
- Aç. Çevre ile hem ısı hem de madde alışverişi yaparlar. Örneğin, yemek bir tencerede açık ateşte pişirilirse, bu açık sistemin canlı bir örneğidir, çünkü tencere dış ortamdan (ateşten) enerji alırken, kendisi de ısı şeklinde enerji yayar. ve su da ondan buharlaşır (metabolizma).
- Kapalı. Bu tür sistemlerde enerji alışverişi olmasına rağmen çevre ile madde alışverişi olmaz. Bir önceki duruma dönersek: kettle'ı bir kapakla kapatırsanız kapalı bir sistem elde edebilirsiniz.
- İzole. Bu, çevredeki boşlukla madde veya enerji alışverişi yapmayan bir tür termodinamik sistemdir. Bir örnek, sıcak çay içeren bir termos olabilir.
Termodinamik sıcaklık

Bu kavram, çevredeki cisimleri oluşturan parçacıkların hızı yansıtan kinetik enerjisi anlamına gelir.parçacıkların rastgele hareketi. Ne kadar büyük olursa, sıcaklık o kadar yüksek olur. Buna göre sistemin kinetik enerjisini az altarak onu soğutuyoruz.
Bu kavram, parçacıkların kaotik hareketinin hızını yansıtan çevreleyen cisimleri oluşturan parçacıkların kinetik enerjisi anlamına gelir. Ne kadar büyük olursa, sıcaklık o kadar yüksek olur. Buna göre sistemin kinetik enerjisini az altarak onu soğutuyoruz.
Termodinamik sıcaklık, Kelvin cinsinden SI (Uluslararası Birimler Sistemi) cinsinden ifade edilir (bu ölçeği ilk öneren İngiliz bilim adamı William Kelvin'in onuruna). Termodinamiğin birinci, ikinci ve üçüncü yasalarını anlamak, sıcaklık tanımı olmadan imkansızdır.
Kelvin ölçeğinde bir derecenin bölümü de bir derece Celsius'a karşılık gelir. Bu birimler arasındaki dönüşüm şu formüle göre gerçekleştirilir: TK =TC + 273, 15, burada TK ve TC - sırasıyla kelvin ve santigrat derece cinsinden sıcaklıklar.
Kelvin ölçeğinin özelliği, negatif değerlere sahip olmamasıdır. İçindeki sıfır (TC=-273, 15 oC), sistemin parçacıklarının termal hareketinin tamamen olmadığı duruma karşılık gelir., "donmuş" görünüyorlar.
Enerjinin korunumu ve termodinamiğin 1. yasası

1824'te Fransız mühendis ve fizikçi Nicolas Léonard Sadi Carnot, yalnızca fiziğin gelişmesine yol açmayan, aynı zamanda teknolojinin gelişmesinde de büyük bir adım haline gelen cesur bir öneride bulundu. Onunşu şekilde formüle edilebilir: "Enerji yaratılamaz veya yok edilemez, sadece bir durumdan diğerine aktarılabilir."
Aslında, Sadi Carnot'un ifadesi, termodinamiğin 1. yasasının temelini oluşturan enerjinin korunumu yasasını varsayar: "Bir sistem dışarıdan enerji aldığında, onu başka biçimlere dönüştürür, ana termal ve mekanik olan."
1. yasanın matematiksel formülü şu şekilde yazılır:
Q=ΔU + A, burada Q, ortamdan sisteme aktarılan ısı miktarıdır, ΔU bu sistemin iç enerjisindeki değişimdir, A mükemmel mekanik iştir.
Adyabatik süreçler
Bunlara iyi bir örnek, dağ yamaçları boyunca hava kütlelerinin hareketidir. Bu tür kütleler çok büyüktür (kilometre veya daha fazla) ve hava mükemmel bir ısı yalıtkanıdır. Belirtilen özellikler, kısa bir süre içinde meydana gelen hava kütleli herhangi bir işlemi adyabatik olarak değerlendirmemize izin verir. Hava bir dağ yamacına çıktığında basıncı düşer, genleşir, yani mekanik iş yapar ve bunun sonucunda soğur. Aksine, hava kütlesinin aşağı doğru hareketine, içindeki basınçta bir artış eşlik eder, sıkışır ve bundan dolayı çok ısınır.
Bir önceki alt başlıkta tartışılan termodinamik yasasının uygulanması, en kolay şekilde adyabatik bir süreç örneği kullanılarak gösterilebilir.
Tanıma göre, bunun sonucunda enerji alışverişi yoktur.çevre, yani yukarıdaki denklemde Q=0. Bu, aşağıdaki ifadeye yol açar: ΔU=-A. Buradaki eksi işareti, sistemin kendi iç enerjisini az altarak mekanik iş yaptığı anlamına gelir. İç enerjinin doğrudan sistemin sıcaklığına bağlı olduğu unutulmamalıdır.
Termal süreçlerin yönü
Bu konu termodinamiğin 2. yasasıyla ilgilidir. Elbette herkes, farklı sıcaklıklardaki iki nesneyi temas ettirirseniz, soğuk olanın her zaman ısınacağını ve sıcak olanın soğuyacağını fark etti. Ters işlemin termodinamiğin birinci yasası çerçevesinde gerçekleşebileceğini, ancak pratikte asla uygulanmadığını unutmayın.
Bu sürecin (ve Evrendeki bilinen tüm süreçlerin) tersinmezliğinin nedeni, sistemin daha olası bir duruma geçişidir. Farklı sıcaklıklardaki iki cismin temasıyla ele alınan örnekte, en olası durum, sistemin tüm parçacıklarının aynı kinetik enerjiye sahip olacağı durumdur.
Termodinamiğin ikinci yasası şu şekilde formüle edilebilir: "Isı asla soğuk bir cisimden sıcak bir cisme kendiliğinden aktarılamaz." Entropi kavramını düzensizliğin bir ölçüsü olarak tanıtacak olursak, bu şu şekilde temsil edilebilir: "Herhangi bir termodinamik süreç entropide bir artışla ilerler".
Isı motoru

Bu terim, kendisine dışarıdan enerji sağlanması nedeniyle mekanik iş yapabilen bir sistem olarak anlaşılır. Birinciısı motorları buhar motorlarıydı ve 17. yüzyılın sonunda icat edildi.
Termodinamiğin ikinci yasası, etkinliklerini belirlemede belirleyici bir rol oynar. Sadi Carnot ayrıca bu cihazın maksimum verimliliğinin şu şekilde olduğunu belirledi: Verimlilik=(T2 - T1)/T2, burada T2 ve T1 ısıtıcı ve buzdolabı sıcaklıklarıdır. Mekanik iş ancak sıcak bir cisimden soğuk cisme bir ısı akışı olduğunda yapılabilir ve bu akış %100 faydalı enerjiye dönüştürülemez.
Aşağıdaki şekil bir ısı motorunun çalışma prensibini göstermektedir (Qabs - makineye aktarılan ısı, Qced - ısı kaybı, W - faydalı iş, P ve V - pistondaki gazın basıncı ve hacmi).
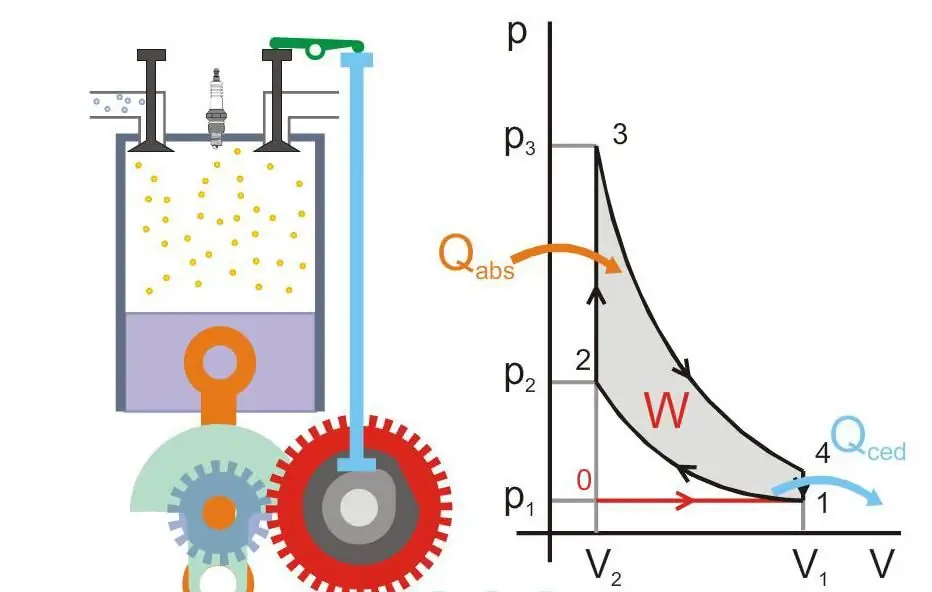
Mutlak sıfır ve Nernst varsayımı
Son olarak, termodinamiğin üçüncü yasasının değerlendirmesine geçelim. Aynı zamanda Nernst postülası olarak da adlandırılır (20. yüzyılın başında ilk kez formüle eden Alman fizikçinin adı). Yasa der ki: "Mutlak sıfıra sınırlı sayıda işlemle ulaşılamaz." Yani, bir maddenin moleküllerini ve atomlarını tamamen "dondurmak" hiçbir şekilde imkansızdır. Bunun nedeni çevre ile sürekli var olan ısı alışverişidir.

Termodinamiğin üçüncü yasasından çıkarılan faydalı bir sonuç, mutlak sıfıra doğru gidildikçe entropinin azalmasıdır. Bu, sistemin kendini organize etme eğiliminde olduğu anlamına gelir. Bu gerçekörneğin, paramanyetleri soğutulduğunda ferromanyetik bir duruma aktarmak için kullanın.
Şimdiye kadar ulaşılan en düşük sıcaklığın 5·10−10 K (2003, MIT laboratuvarı, ABD) olduğunu belirtmek ilginçtir.






